Sind wir jetzt bei Facebook?Like NI2
Reaktion von Ascorbinsäure mit Vanillin als Lösungsmittel
Moderatoren: Moderatoren, Assistenten
- frankie
- Illum.-Ass.
- Beiträge: 1941
- Registriert: Dienstag 10. April 2007, 17:00
- Wohnort: Res Publica Austria
Afaik ist Jans Hydraulikpresse noch nicht komplett, ja ? Aber ne kleine SC wäre vlt. machbar ...Evtl. kristallisieren lassen, dann versuchen in der Säule ein paar Fraktionen zu trennen, rekristallisieren und nen KBr-Pressling?
mfg
It is always better to have no ideas than false ones; to believe nothing, than to believe what is wrong.
(Thomas Jefferson)
(Thomas Jefferson)
Hat eigentlich schonmal jemand an ne DC gedacht? 
I❤OC
There is no sadder sight in the world than to see a beautiful theory killed by a brutal fact. [T. Huxley]
The pursuit of knowledge is hopeless and eternal. Hooray! [Prof. H. J. Farnsworth]
Trust the rhythm and the rhyme of your own heartbeat. [C. Douglas]
There is no sadder sight in the world than to see a beautiful theory killed by a brutal fact. [T. Huxley]
The pursuit of knowledge is hopeless and eternal. Hooray! [Prof. H. J. Farnsworth]
Trust the rhythm and the rhyme of your own heartbeat. [C. Douglas]
- Cyanwasserstoff
- Illumina-Admin
- Beiträge: 6303
- Registriert: Sonntag 7. Mai 2006, 20:41
- Kontaktdaten:
Gerne; freut mich.Ich möchte dir, Cyan und allen anderen Illumina-Mitgliedern die tatkräftig zur Lösung versucht haben beizutragen, auf alle Falle schon mal für die großartige Hilfe danken. Und das ist wirklich ganz ernst gemeintBin stolz, hier zu sein...
@ Hannes: Ja, hab ich, aber gestern keine Zeit gehabt und jetzt hab ich kein Vanillin mehr.
Ich habe keine Hydraulikpresse mehr. Nachdem sie undicht war, ich sie auseinandergenommen habe und festgestellt habe, dass die Dichtung scheinbar eine Spezialanfertigung ist und ich eine NaCl-Küvette ergattert habe, habe ich die Presse verkauft. In die Küvette kommen mir vorsichtshalber aber nur aprotische, ausreichend genau definierbare Substanzen rein.
"It is arguably true that the tetrapyrrole system is Nature's most remarkable creation."
- Claude Rimington
- Claude Rimington
- Newclears
- Illumina-Moderator
- Beiträge: 4997
- Registriert: Montag 10. August 2009, 15:48
- Wohnort: Alt-Erschwede
Wahl des Laufmittels ist immer etwas schwierig. Ich würde es erstmal mit nem Gemisch aus EtOH, Wasser und Essigsäure probieren. Verhältnis empirisch ermitteln. Wenn das keine zufriedenstellende Trennung bringt mit nem ziemlich aprotischen und apolarem Gemisch z.B. DCM oder TCM, Hexan und 1- Propanol oder 1- Butanol als 2D versuchen. Damit deckst Du beide Möglichkeiten auf einer Platte ab und kannst dich weiter vortasten. Tabellierte Rf Werte wird es für das/ die Produkte nicht geben.
"...wie ein Sprecher betont,hat für die Bevölkerung zu keinem Zeitpunkt Gefahr bestanden."
"...mittlerweile rostet das Miststück..." E.v. Däniken
"...mittlerweile rostet das Miststück..." E.v. Däniken
Ne 2D DC wäre eh zu empfehlen (weil ich denke, dass das Produktgemisch recht komplex sein könnte), allerdings solltest du (Markus) die ersten DCs mit deinen Edukten machen, da kannste erstmal mit den Laufmitteln experimentieren und kommst an ein paar R__f__-Werte und kannst gleich die Reinheit überprüfen, und evtl. Verunreinigungen ausmachen, vll enthält ja jedes kommerzielle Vanillin gewisse Anteile (ja nach Lagerung) der Säure - ich bin mir nicht sicher wie oxidationsbeständig Vanillin ist. Da wäre vielleicht nach aussagekräftiger DC noch eine extra Reinigung nötig... *wie ich Analytik hasse* ^^
I❤OC
There is no sadder sight in the world than to see a beautiful theory killed by a brutal fact. [T. Huxley]
The pursuit of knowledge is hopeless and eternal. Hooray! [Prof. H. J. Farnsworth]
Trust the rhythm and the rhyme of your own heartbeat. [C. Douglas]
There is no sadder sight in the world than to see a beautiful theory killed by a brutal fact. [T. Huxley]
The pursuit of knowledge is hopeless and eternal. Hooray! [Prof. H. J. Farnsworth]
Trust the rhythm and the rhyme of your own heartbeat. [C. Douglas]
- Newclears
- Illumina-Moderator
- Beiträge: 4997
- Registriert: Montag 10. August 2009, 15:48
- Wohnort: Alt-Erschwede
Grade bei Wikipedia in einem Bildkommentar gefunden:
http://de.wikipedia.org/w/index.php?tit ... 0403124641
Vanillin kann also neMenge bunte Sachen. Interessant finde ich in demKontext hier besonders den gelbgrünen Spot an der Startlinie. (dritter von rechts)The scan of TLC plate (silica gel G) with 10 essential oils developed with mobile phase toluene - ethyl acetate (93:7 v/v), next sprayed with vanillin in H2SO4 and heated. From left to right oils from: bergamot, cedar, eucalyptus, syzygium, malaleuca, lav
http://de.wikipedia.org/w/index.php?tit ... 0403124641
"...wie ein Sprecher betont,hat für die Bevölkerung zu keinem Zeitpunkt Gefahr bestanden."
"...mittlerweile rostet das Miststück..." E.v. Däniken
"...mittlerweile rostet das Miststück..." E.v. Däniken
- MarkusB
- Illumina-Mitglied
- Beiträge: 79
- Registriert: Samstag 12. November 2011, 03:14
- Wohnort: Shanghai
Ja, wie ich anfangs geschrieben habe. Gefunden habe ich (bis jetzt) aber nur die sogenannte Günzburg-Reagenz (Gemisch aus Lösungen von Phlorogluzin u. Vanillin in Alkohol) zum Nachweis kleinster Mengen freier Salzsäure sowie eine Reagenz, die aus Vanillin und Schwefelsäure besteht, um u. a. Steroide nachzuweisen.Newclears hat geschrieben:Vanillin kann also ne Menge bunte Sachen.
Zur Reinigung des Vanillins könnte ich dessen Sublimationsverhalten ausnutzen. Besorge mir mal ne DC-Ausrüstung. Mal sehen, was es hier so gibt. Hab' das lange nicht mehr gemacht.NI2 hat geschrieben:Da wäre vielleicht nach aussagekräftiger DC noch eine extra Reinigung nötig... *wie ich Analytik hasse* ^^
Noch schönen Sonntag,
Markus
"I'm an explorer okay, I get curious about everything and I want to investigate all kinds of stuff." (Richard Phillips Feynman)
- MarkusB
- Illumina-Mitglied
- Beiträge: 79
- Registriert: Samstag 12. November 2011, 03:14
- Wohnort: Shanghai
Ein weiteres Experiment...
Eingedampfte Dehydroascorbinsäure:
Ziemlich klebrig im noch feuchten Zustand und gelblich-grün.
1 g der getrockneten Dehydroascorbinsäure wurde dann mit 3 g Vanillin vermischt und im Wasserbad auf 90 °C erwärmt, um partielle Überhitzung und weitere thermische Zersetzung vorzubeugen.

Die Dehydroascorbinsäure löste sich jedoch nicht im Vanillin, ein bräunliches Stoffgemisch resultierte:

Die Reaktion zwischen Ascorbinsäure und Vanillin ist meiner Ansicht nach bereits während der Protonen- bzw. Elektronenabgabe der Ascorbinsäure zu suchen. Nach Abgabe beider Protonen entsteht aus Ascorbinsäure ein Dianion (Asc2−). Ascorbinsäure kann aber auch nur ein Elektron und Protons abgeben (AscH.); in diesem Zustand ist sie eine sehr starke Säure (pKs = −0,45). Im wässrigen Medium spielt das normalerweise wegen der Kurzlebigkeit keine Rolle, anders kann dies gelöst in Vanillin ablaufen.
Eingedampfte Dehydroascorbinsäure:

Ziemlich klebrig im noch feuchten Zustand und gelblich-grün.
1 g der getrockneten Dehydroascorbinsäure wurde dann mit 3 g Vanillin vermischt und im Wasserbad auf 90 °C erwärmt, um partielle Überhitzung und weitere thermische Zersetzung vorzubeugen.

Die Dehydroascorbinsäure löste sich jedoch nicht im Vanillin, ein bräunliches Stoffgemisch resultierte:

Die Reaktion zwischen Ascorbinsäure und Vanillin ist meiner Ansicht nach bereits während der Protonen- bzw. Elektronenabgabe der Ascorbinsäure zu suchen. Nach Abgabe beider Protonen entsteht aus Ascorbinsäure ein Dianion (Asc2−). Ascorbinsäure kann aber auch nur ein Elektron und Protons abgeben (AscH.); in diesem Zustand ist sie eine sehr starke Säure (pKs = −0,45). Im wässrigen Medium spielt das normalerweise wegen der Kurzlebigkeit keine Rolle, anders kann dies gelöst in Vanillin ablaufen.
"I'm an explorer okay, I get curious about everything and I want to investigate all kinds of stuff." (Richard Phillips Feynman)
- MarkusB
- Illumina-Mitglied
- Beiträge: 79
- Registriert: Samstag 12. November 2011, 03:14
- Wohnort: Shanghai
Habe von der LAT GmbH ein IR-Spektrum der Schmelze als KBr-Preßling erstellen lassen. Die Schmelze konnte problemlos hergestellt werden und war von der Färbung her wie beschrieben. Allerdings ist diese beim Abkühlen auch erstarrt.
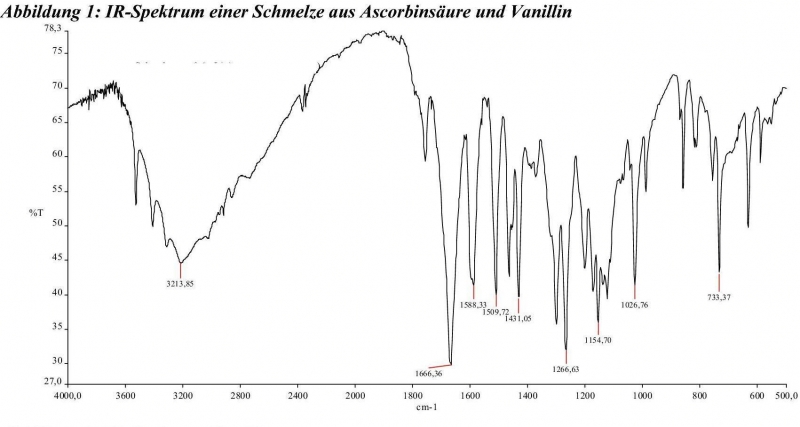



Herr Dr. Larisch, stellv. technischer Direktor der LAT und Autor des Buches Beiträge zur Maillard-Reaktion der Ascorbinsäure hat mich hier sehr freundlich und sachkundig unterstützt.
Nach Meinung von Herrn Dr. Larisch sieht der Sachverhalt wie folgt aus:
Im IR-Spektrum des Reaktionsgemisches lassen sich die Banden für Vanillin und Ascorbinsäure finden. Das liegt daran, dass mit großer Wahrscheinlichkeit nur ein sehr geringer Teil der Ausgangsstoffe Vanillin und Ascorbinsäure zu anderen Verbindungen u.a, der auffälligen grünen Verbindung umgesetzt ist, die natürlich wegen ihrer Färbung rein optisch dominiert. Zum Anderen können die potentiellen Reaktionsprodukte natürlich auch die Strukturen von Ascorbinsäure und Vanillin enthalten (z. B. der Ester) die dann auch die entsprechenden Banden zeigen. Insofern lässt sich aus dem IR-Spektrum keine Aussage über die mögliche Identität/Struktur der grünen Verbindung ableiten.
Um weiter voranzukommen müsste das Reaktionsgemisch mittels chromatographischer Methoden (HPLC) getrennt und analysiert werden. Hier ließe sich über online aufgenommene DAD-Spektren (UV-Spektren) ggf. die grüne Verbindung einem Peak zuordnen. Anschließend müsste man Reaktionsbedingungen finden unter denen die grüne Verbindung in starkem Maße bzw. als Hauptprodukt entsteht.
Sie könnte dann mittels Säulenchromatographie und/oder präparativer DC und/oder präparativer HPLC angereichert und gereinigt werden.
Wenn sie gereinigt und als Substanz fassbar ist (nach meinen Erfahrungen sind manche Substanzen, die aus Ascorbinsäure entstehen leicht oxidierbar und als Reinsubstanzen äußerst instabil, d.h. sie bauen ab bzw. reagieren weiter wenn sie nicht im Gemisch vorliegen) könnte dann eine Strukturaufklärung mittels spektroskopischer Methoden (H-NMR, C-NMR, H-H-COSY, MS; UV; IR...) erfolgen.




Herr Dr. Larisch, stellv. technischer Direktor der LAT und Autor des Buches Beiträge zur Maillard-Reaktion der Ascorbinsäure hat mich hier sehr freundlich und sachkundig unterstützt.
Nach Meinung von Herrn Dr. Larisch sieht der Sachverhalt wie folgt aus:
Im IR-Spektrum des Reaktionsgemisches lassen sich die Banden für Vanillin und Ascorbinsäure finden. Das liegt daran, dass mit großer Wahrscheinlichkeit nur ein sehr geringer Teil der Ausgangsstoffe Vanillin und Ascorbinsäure zu anderen Verbindungen u.a, der auffälligen grünen Verbindung umgesetzt ist, die natürlich wegen ihrer Färbung rein optisch dominiert. Zum Anderen können die potentiellen Reaktionsprodukte natürlich auch die Strukturen von Ascorbinsäure und Vanillin enthalten (z. B. der Ester) die dann auch die entsprechenden Banden zeigen. Insofern lässt sich aus dem IR-Spektrum keine Aussage über die mögliche Identität/Struktur der grünen Verbindung ableiten.
Um weiter voranzukommen müsste das Reaktionsgemisch mittels chromatographischer Methoden (HPLC) getrennt und analysiert werden. Hier ließe sich über online aufgenommene DAD-Spektren (UV-Spektren) ggf. die grüne Verbindung einem Peak zuordnen. Anschließend müsste man Reaktionsbedingungen finden unter denen die grüne Verbindung in starkem Maße bzw. als Hauptprodukt entsteht.
Sie könnte dann mittels Säulenchromatographie und/oder präparativer DC und/oder präparativer HPLC angereichert und gereinigt werden.
Wenn sie gereinigt und als Substanz fassbar ist (nach meinen Erfahrungen sind manche Substanzen, die aus Ascorbinsäure entstehen leicht oxidierbar und als Reinsubstanzen äußerst instabil, d.h. sie bauen ab bzw. reagieren weiter wenn sie nicht im Gemisch vorliegen) könnte dann eine Strukturaufklärung mittels spektroskopischer Methoden (H-NMR, C-NMR, H-H-COSY, MS; UV; IR...) erfolgen.
"I'm an explorer okay, I get curious about everything and I want to investigate all kinds of stuff." (Richard Phillips Feynman)
- frankie
- Illum.-Ass.
- Beiträge: 1941
- Registriert: Dienstag 10. April 2007, 17:00
- Wohnort: Res Publica Austria
Es war mir irgendwo klar, dass sich der Sachverhalt in Messung in etwa so äußern würde ... die Interpretation des Herrn Dr. Larisch teile ich. Ich finde es jedoch absolut Klasse, dass du dir diese Arbeit angetan hast  Von wegen es existiere keine Forschung im privaten Bereich ...
Von wegen es existiere keine Forschung im privaten Bereich ...
mfg
mfg
It is always better to have no ideas than false ones; to believe nothing, than to believe what is wrong.
(Thomas Jefferson)
(Thomas Jefferson)
- MarkusB
- Illumina-Mitglied
- Beiträge: 79
- Registriert: Samstag 12. November 2011, 03:14
- Wohnort: Shanghai
Ich hatte meine Arbeit hierzu bei CHIUZ eingereicht. Heute kam die Absage per Email mit folgender Begründung:
Sehr geehrter Herr ...,
nach Rücksprache mit zwei mit den Belangen der Zeitschrift vertrauten Beratern muss ich Ihnen leider mitteilen, dass wir Ihren Beitrag nicht zur Publikation in der Chemie in unserer Zeit annehmen können. Die Zeitschrift publiziert keine Originalarbeiten, um eine solche handelt es sich bei Ihrem Beitrag.
Mit freundlichen Grüßen und den besten Wünschen für das kommende Jahr
...
Was ist davon zu halten?
Sehr geehrter Herr ...,
nach Rücksprache mit zwei mit den Belangen der Zeitschrift vertrauten Beratern muss ich Ihnen leider mitteilen, dass wir Ihren Beitrag nicht zur Publikation in der Chemie in unserer Zeit annehmen können. Die Zeitschrift publiziert keine Originalarbeiten, um eine solche handelt es sich bei Ihrem Beitrag.
Mit freundlichen Grüßen und den besten Wünschen für das kommende Jahr
...
Was ist davon zu halten?
"I'm an explorer okay, I get curious about everything and I want to investigate all kinds of stuff." (Richard Phillips Feynman)
-
t0bychemie
- Illum.-Ass.
- Beiträge: 1056
- Registriert: Freitag 4. Januar 2008, 11:23
- Kontaktdaten:
Ich verstehe den Begriff "Originalarbeit" nicht wirklich. Was ist damit konkret gemeint? Vielleicht geht es darum, dass die Zeitschrift nicht selbst recherchiert hat..?
Interessenvereinigung Naturwissenschaft und Technik IVNT e.V.
Der Verein für alle, die gerne selbst forschen und experimentieren.
Homepage: www.ivnt.de

Der Verein für alle, die gerne selbst forschen und experimentieren.
Homepage: www.ivnt.de
