Hier wird die Synthese des Hexaphenylbenzols durch Diels-Alder-Reaktion von Tetraphenylcyclopentadienon mit Diphenylacetylen gefolgt von der Eliminierung von Kohlenstoffmonooxid beschrieben.
Geräte:
Reagenzglas, Reagenzglashalter, Bunsenbrenner, Apparatur zur Vakuumfiltration, Waage, Spatel
Chemikalien:
Tetraphenylcyclopentadienon
Diphenylacetylen (Tolan)
Siliconöl
n-Pentan



Toluol
Hexaphenylbenzol
Hinweis:
Es ist im Abzug zu arbeiten!
Durchführung:
0,40 g Tetraphenylcyclopentadienon und 0,40 g Diphenylacetylen werden in einem Reagenzglas in 4 ml Siliconöl suspendiert. Nun erhitzt man mit dem Bunsenbrenner so stark, dass kräftige Blasenbildung erkennbar ist. Dabei wandelt sich die Farbe langsam von weinrot nach gelbbraun um. Man lässt abkühlen, verrührt mit 10 ml n-Pentan und saugt den ausgefallenen Niederschlag ab, der nun noch zweimal mit je 5 ml n-Pentan, einmal mit 5 ml Toluol und noch einmal mit 5 ml n-Pentan nachgewaschen wird. Ausbeute: 0,42 g (76% d.Th.) Hexaphenylbenzol. Weißes bis schwach graues Pulver.
Entsorgung:
Reste gibt man zu den organischen Abfällen. n-Pentan und Toluol werden zu den halogenfreien organischen Lösemittelabfällen gegeben.
Erklärung:
Zunächst findet eine Diels-Alder-Reaktion zwischen Tetraphenylcyclopentadienon (Dien) und Diphenylacetylen (Dienophil) statt, woraufhin durch Eliminierung von Kohlenstoffmonooxid Hexaphenylbenzol gebildet wird:
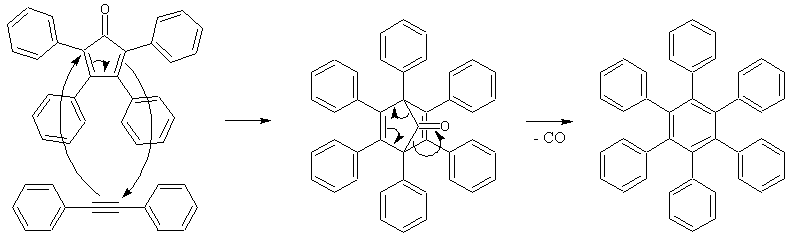
Bild:

Vor dem Erhitzen

Zu Beginn der Reaktion liegt eine weinrote Lösung vor.

Nach der Reaktion

Hexaphenylbenzol
