Siedepunkt eines "Reinstoffes" stark abweichend
Moderator: Moderatoren
-
CD-ROM-LAUFWERK
- Illumina-Mitglied
- Beiträge: 581
- Registriert: Sonntag 5. Januar 2014, 23:05
Siedepunkt eines "Reinstoffes" stark abweichend
Das Azeotrop Ethanol/Wasser (ziemlich genau 90 mol% Ethanol) sollte bei 1013,15hPa und 78,14°C sieden.
Ich habe bei 1031,5hPa nur 77,35°C gemessen, bei dem Druck sollten es jedoch schon 78,60°C sein.
Die Druckmessung ist absolut mind. auf 1 hPa genau. Refferenz war kürzlich ein Quecksilberbarometer, gemessen 1012,8hPa bei einer Ableseungenauigkeit von etwa +-1hPa ggü. meinem Sensor (BME280) mit 1012,14hPa. Der Druck schwankte im Verlauf (2h) der Destillation um 0,5hPa.
Das Thermometer ist laut Kalibrierschein von vor 3 Monaten absolut auf 0,001°C genau. In Schnee+Wasser messe ich -0,04°C, wobei ich da von einer Verfälschung durch Salze ausgehe.
Die Messfehler zusammen erlauben keine derartigen Abweichung. Der Druck müsste für diese Temperatur bei 983hPa liegen bzw. das Thermometer solide 1,3°C zu wenig anzeigen. Es gibt im Siedebereich von Ethanol+Wasser keine niedrigere Temperatur als den azeotropen Punkt.
Wie sind die Abweichungen zu erklären? Hat jemand eine Idee?
Einzig eine Unterkühlung des Dampfes wäre eine Erklärung. Jedoch sollte eine Kondensation unter diesen Bedingungen* alles andere als gehindert sein?!
*Hydrophiles Glas bzw. Edelstahl für den Sensor und alles vollständig benetzt, Messpunkt direkt nach einer Kolonne mittig im starken Dampfstrom
Nebenfrage: Wie fittet ihr Kurven? Mit Excel stoße ich schnell an meine Grenzen, mit der RGP-Funktion kann ich irgendwie beim Polynom keine Potenzen >5 machen, da ich dann einfach immer mehr 0-Werte für Koeffizienten bekomme. Das Fitting im Diagramm selbst ist relativ nutzlos für die Punkte, da sind leider große Abweichungen.
Auch XURU gibt mir da nicht ohne weiteres (ganz viele einzelne Abschnitte) passende Ergebnisse, wobei da irgendwie auch immer die Parameter auf 2 beschränkt werden.
Ansonsten zeigt sich bei der Vermessung einer Kolonne, dass die größte Ungenauigkeit bei Weitem das Rücklaufverhältnis ist. Kleinste Schwankungen überdecken alles andere. Und generell ist die Temperaturmessung über ein digitales Thermometer deutlich geeigneter. Eine Auflösung von 0,01°C ist dabei wünschenswert und zeigt einem schon kleinste Konzentrationsunterschiede, wo Dichte oder Brechungsindex noch weit davon entfernt sind einen Unterschied zu messen.
Ich habe bei 1031,5hPa nur 77,35°C gemessen, bei dem Druck sollten es jedoch schon 78,60°C sein.
Die Druckmessung ist absolut mind. auf 1 hPa genau. Refferenz war kürzlich ein Quecksilberbarometer, gemessen 1012,8hPa bei einer Ableseungenauigkeit von etwa +-1hPa ggü. meinem Sensor (BME280) mit 1012,14hPa. Der Druck schwankte im Verlauf (2h) der Destillation um 0,5hPa.
Das Thermometer ist laut Kalibrierschein von vor 3 Monaten absolut auf 0,001°C genau. In Schnee+Wasser messe ich -0,04°C, wobei ich da von einer Verfälschung durch Salze ausgehe.
Die Messfehler zusammen erlauben keine derartigen Abweichung. Der Druck müsste für diese Temperatur bei 983hPa liegen bzw. das Thermometer solide 1,3°C zu wenig anzeigen. Es gibt im Siedebereich von Ethanol+Wasser keine niedrigere Temperatur als den azeotropen Punkt.
Wie sind die Abweichungen zu erklären? Hat jemand eine Idee?
Einzig eine Unterkühlung des Dampfes wäre eine Erklärung. Jedoch sollte eine Kondensation unter diesen Bedingungen* alles andere als gehindert sein?!
*Hydrophiles Glas bzw. Edelstahl für den Sensor und alles vollständig benetzt, Messpunkt direkt nach einer Kolonne mittig im starken Dampfstrom
Nebenfrage: Wie fittet ihr Kurven? Mit Excel stoße ich schnell an meine Grenzen, mit der RGP-Funktion kann ich irgendwie beim Polynom keine Potenzen >5 machen, da ich dann einfach immer mehr 0-Werte für Koeffizienten bekomme. Das Fitting im Diagramm selbst ist relativ nutzlos für die Punkte, da sind leider große Abweichungen.
Auch XURU gibt mir da nicht ohne weiteres (ganz viele einzelne Abschnitte) passende Ergebnisse, wobei da irgendwie auch immer die Parameter auf 2 beschränkt werden.
Ansonsten zeigt sich bei der Vermessung einer Kolonne, dass die größte Ungenauigkeit bei Weitem das Rücklaufverhältnis ist. Kleinste Schwankungen überdecken alles andere. Und generell ist die Temperaturmessung über ein digitales Thermometer deutlich geeigneter. Eine Auflösung von 0,01°C ist dabei wünschenswert und zeigt einem schon kleinste Konzentrationsunterschiede, wo Dichte oder Brechungsindex noch weit davon entfernt sind einen Unterschied zu messen.
-
Glaskocher
- Illumina-Mitglied
- Beiträge: 2544
- Registriert: Dienstag 27. Oktober 2015, 22:17
- Wohnort: Leverkusen
Die Geräte scheinen tadellos zu sein.
Wie sieht es mit dem Alkohol und dem Wasser aus? Waren das auch p.A. Substanzen oder enthielt das Ethanol ein Vergällungsmittel? Hast Du das Ganze mal in einige gleichgroße Fraktionen destillativ aufgeteilt? Eventuell läßt sich dann ein Trend erkennen, ob da noch Leichtsieder in den ersten Fraktionen mit drin sind. Allerdings benutzt man gerne Vergällungszusätze, die sich nur schlecht abtrennen lassen.
Hast Du irgendeine unabhängige Analytik zur Verfügung, um die Organika im Destillationsgut bestimmen zu können? Das könnte das Rätsel lösen, oder zumindest Hinweise geben.
Wie sieht es mit dem Alkohol und dem Wasser aus? Waren das auch p.A. Substanzen oder enthielt das Ethanol ein Vergällungsmittel? Hast Du das Ganze mal in einige gleichgroße Fraktionen destillativ aufgeteilt? Eventuell läßt sich dann ein Trend erkennen, ob da noch Leichtsieder in den ersten Fraktionen mit drin sind. Allerdings benutzt man gerne Vergällungszusätze, die sich nur schlecht abtrennen lassen.
Hast Du irgendeine unabhängige Analytik zur Verfügung, um die Organika im Destillationsgut bestimmen zu können? Das könnte das Rätsel lösen, oder zumindest Hinweise geben.
-
CD-ROM-LAUFWERK
- Illumina-Mitglied
- Beiträge: 581
- Registriert: Sonntag 5. Januar 2014, 23:05
Zur Qualität des Thermometers: Folgend ~300'000 Messpunkte.
Gemessen wurde die Temperatur von Eiswasser (aus Schnee von draußen) in einem isolierten Eimer.
Es handelte sich um 7kg, davon etwa 50% als Eis und 50% Schmelzwasser. Bis zum vollständigen Schmelzen vergingen etwa 2,5 Tage, da der Wärmestrom in den Eimer sich nur auf etwa 4W beläuft.
Der Eimer wurde nicht gerührt, da ein Rührer schon erhebliche Wärmemengen eintragen würde. Der Temperaturfühler war immer mitten im aufschwimmenden Schnee. Der Mittelwert der Temperatur liegt bei 0,069°C.
Danach eine Normalverteilung der Schwankung der Messwerte als Glockenkurve, die Standardabweichung selbiger liegt bei 2,1mK.
Nach dem vollständigen schmelzen des Schnees dann noch der schöne Verlauf der extrem langsam steigenden Temperatur (etwa 0,3°C pro Stunde).


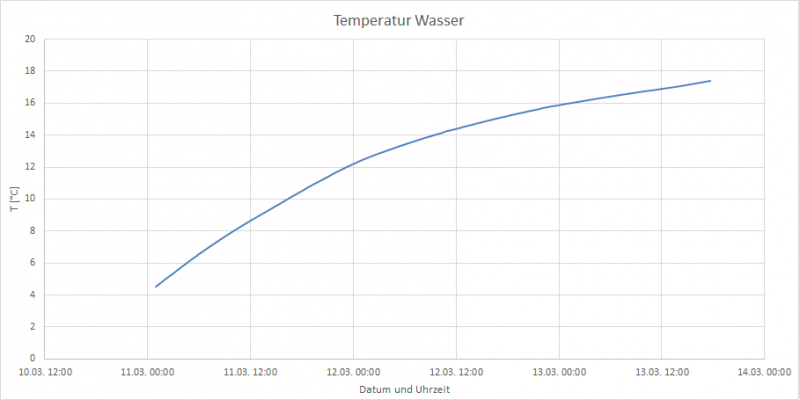
Gemessen wurde die Temperatur von Eiswasser (aus Schnee von draußen) in einem isolierten Eimer.
Es handelte sich um 7kg, davon etwa 50% als Eis und 50% Schmelzwasser. Bis zum vollständigen Schmelzen vergingen etwa 2,5 Tage, da der Wärmestrom in den Eimer sich nur auf etwa 4W beläuft.
Der Eimer wurde nicht gerührt, da ein Rührer schon erhebliche Wärmemengen eintragen würde. Der Temperaturfühler war immer mitten im aufschwimmenden Schnee. Der Mittelwert der Temperatur liegt bei 0,069°C.
Danach eine Normalverteilung der Schwankung der Messwerte als Glockenkurve, die Standardabweichung selbiger liegt bei 2,1mK.
Nach dem vollständigen schmelzen des Schnees dann noch der schöne Verlauf der extrem langsam steigenden Temperatur (etwa 0,3°C pro Stunde).



- mgritsch
- Illumina-Admin
- Beiträge: 4385
- Registriert: Montag 8. Mai 2017, 10:26
- Wohnort: in den Misanthropen
Re: Siedepunkt eines "Reinstoffes" stark abweichen
mhhh... eine Druckangabe von 1031 hPa erscheint mir ungewöhnlich, das ist Meteorologisch gesehen schon extremer Hochdruck. Ich weiß ja nicht wo du beheimatet bist, aber zb hier http://www.niederschlagsradar.de/wetter ... irPressure kann man jede Menge Luftdruckverläufe abrufen und im März lag der Luftdruck in München, Köln und Frankfurt zwischen min 990 und max 1015 mbar, in Dresden und Hamburg gabs zu Monatsanfang mal eine Sptzenwert von 1019 bzw 1021 mbar. Von daher hab ich den leisen Verdacht dass an dem Wert etwas nicht stimmt. Check mal deine Location und Datum der Messung gegen diese offiziellen meteorologischen Werte... (wobei es natürlich immer sein kann dass in deinem Gebäude durch eine entsprechende Belüftungsanlage ein lokaler Überdruck herrscht...)CD-ROM-LAUFWERK hat geschrieben:Das Azeotrop Ethanol/Wasser (ziemlich genau 90 mol% Ethanol) sollte bei 1013,15hPa und 78,14°C sieden.
Ich habe bei 1031,5hPa nur 77,35°C gemessen, bei dem Druck sollten es jedoch schon 78,60°C sein.
Die Druckmessung ist absolut mind. auf 1 hPa genau. Refferenz war kürzlich ein Quecksilberbarometer, gemessen 1012,8hPa bei einer Ableseungenauigkeit von etwa +-1hPa ggü. meinem Sensor (BME280) mit 1012,14hPa. Der Druck schwankte im Verlauf (2h) der Destillation um 0,5hPa.
Unterkühlung muss nicht mit Kondensation einhergehen! Kristallistions-/Kondensationshemmung ist nichts ungewöhnliches.Wie sind die Abweichungen zu erklären? Hat jemand eine Idee?
Einzig eine Unterkühlung des Dampfes wäre eine Erklärung. Jedoch sollte eine Kondensation unter diesen Bedingungen* alles andere als gehindert sein?!
*Hydrophiles Glas bzw. Edelstahl für den Sensor und alles vollständig benetzt, Messpunkt direkt nach einer Kolonne mittig im starken Dampfstrom
Bei jeder Labor-Destillationsapparatur die ich kenne hängen am Thermometer Tropfen bzw bildet sich ein gewisser Rückfluss, das ist jedenfalls ein Hinweis dass man an diesem Messpunkt im Bereich leicht unter dem Taupunkt ist.
Ein polynomischer fit macht nur sinn, wenn der zugrundeliegende Zusammenhang zwischen unabhängiger und abhängiger Variable auch einer polynomischen Gesetzmäßigkeit folgt. Ich weiß jetzt nicht welche Daten du genau fitten willst, aber wenn es sowas ist wie die 300.000 Punkt zur Wassertermperatur - das macht überhaupt keinen Sinn.0-Werte für Koeffizienten geben auch eine mathematisch klare Antwort - der Term ist statistisch bereits bedeutungslos für das Ergebnis, also eh schon alles perfekt... Was willst du mit dem Fit erreichen? einfach glätten? Dann mach moving average. Es gibt einen kopmplexeren mathematischen Zusammenhand der nicht angeboten wird? Dann transformiere deine Messwerte so dass sie einer der angebotenen Funktionstypen entsprechen...Nebenfrage: Wie fittet ihr Kurven? Mit Excel stoße ich schnell an meine Grenzen, mit der RGP-Funktion kann ich irgendwie beim Polynom keine Potenzen >5 machen, da ich dann einfach immer mehr 0-Werte für Koeffizienten bekomme. Das Fitting im Diagramm selbst ist relativ nutzlos für die Punkte, da sind leider große Abweichungen.
Auch XURU gibt mir da nicht ohne weiteres (ganz viele einzelne Abschnitte) passende Ergebnisse, wobei da irgendwie auch immer die Parameter auf 2 beschränkt werden.
-
CD-ROM-LAUFWERK
- Illumina-Mitglied
- Beiträge: 581
- Registriert: Sonntag 5. Januar 2014, 23:05
Kondensationshemmung an einem bereits vom Medium benetzten Ort? Kannst du das mit einer Quelle belegen? Ich bin kein Materialwissenschaftler, aber ich kann es mir einfach nicht vorstellen, dass soetwas möglich wäre. Nehmen wir aber mal an, dass der Dampf nicht gerne dort kondensieren will: Das müsste irgendwie über 1°C Temperaturdifferenz verursachen. Der Messfühler ragt ~3cm tief in den Gasstom und noch mal ~5cm in stagnierenden Dampf. D.h. es müsste vom Fühler ein Wärmestrom nach außen führen und über die ~8cm des Messfühlers an der Spitze für diesen Temperaturabfall sorgen. Das halte ich für ausgeschlossen. Der Dampf muss nach einer 40cm Füllkörperkolonne (bei unendlichem Rückflussverhältnis, also 100% gehen wieder zurück) im Gleichgewicht sein. Eine "Möglichkeit" wäre, dass der Rückfluss den Dampf (der unter dem Thermometer direkt auf die Kolonne geht) "abkühlt".Unterkühlung muss nicht mit Kondensation einhergehen! Kristallistions-/Kondensationshemmung ist nichts ungewöhnliches.
Der Beitrag ist von Januar 2017, die Messung war im Dezember.und im März
Bitte beachten, dass die Werte oftmals als auf Meereshöhe reduzierte Drücke angegeben sind. (OT: Hier gibt es Messwerte von [allen?] Wetterstationen)
Hier spezifisch für den Ort und Zeitpunkt des eingangs genannten Versuchs, peak in dem Zeitraum war bei etwa 1040hPa.
Das Thermometer wird auch nicht erst nach einem aufwärmen in den Dampfstrom geführt, also muss sich selbstverständlich Kondensat darauf bilden, um das Thermometer selbst zu erwärmen. Ein kleines bisschen Wärmestrahlung wird vermutlich pausenlos einen sehr kleinen Wärmestrom abführen. Ansonsten kann die Wärme nur über das Thermometer selbst nach außen (im Glas) geleitet werden, was in Anbetracht der geringen Wärmeleitfähigkeit von Glas keine Rolle spielen kann.Bei jeder Labor-Destillationsapparatur die ich kenne hängen am Thermometer Tropfen bzw bildet sich ein gewisser Rückfluss, das ist jedenfalls ein Hinweis dass man an diesem Messpunkt im Bereich leicht unter dem Taupunkt ist.
Jedenfalls stimmt es auch mit einem Quecksilberbarometer auf den Ablesefehler überein (Siehe Bild unten). Selbiges mit 5 bis 6 verschiedenen dieser Sensoren, sie weichen nur der Hestellerangabe (1hPa) folgend absolut etwas voneinander ab (relativ gibt es keinen signifikaten Messfehler). Derartige absolute Abweichungen vom Realwert (also ~20hPa, damit die Temperatur stimmen würde) sind ausgeschlossen. Der Wert unten links auf dem OLED-Display ist in mbar/hPa. Das Manometer steht bei etwas unter 101,3kPa, vielleicht 101,28kPa.Von daher hab ich den leisen Verdacht dass an dem Wert etwas nicht stimmt.

Zum Thema Daten fitten: TableCurve 2D.
Etwas besseres habe ich auch im Rahmen meiner Bachelorarbeit nicht gefunden, wo die Modellierung von Daten praktisch der Kernpunkt war.
Ursprünglich ging es darum, den Verlauf des Brechungsindexes über den Ethanolanteil als Funktion zu haben mit möglichst wenig Abweichungen. Zwecks einfacher Berechnung des Ethanolanteils anhand des Brechungsindex. Dafür hätte auch ein Polynom gereicht. Dass die höheren Koeffizienten null waren ist eine reine Limitierung seitens Excel, das hat nichts mit der Mathematik zu tun. Mit TableCurve 2D kann einfach auch deutlich sinnvollere Funktionen finden und fitten. Diese sind mit 3-4 Parametern viel besser als jedes Polynom.
- mgritsch
- Illumina-Admin
- Beiträge: 4385
- Registriert: Montag 8. Mai 2017, 10:26
- Wohnort: in den Misanthropen
ah, ok... dass das aus dem Jan war hatte ich übesehen.
auf Meereshöhe reduziert: lass dich von dem Begriff nicht irritieren! Bei höhne < 0m (was in DE überwiegend der Fall ist) ergibt sich dabei ein rechnerisch höherer Luftdruck als der absolute, gemessene!
Naja, wenn alle Messungen perfekt sind dann kann es wohl nur noch ein Naturwunder sein. Was soll man da noch sagen.
auf Meereshöhe reduziert: lass dich von dem Begriff nicht irritieren! Bei höhne < 0m (was in DE überwiegend der Fall ist) ergibt sich dabei ein rechnerisch höherer Luftdruck als der absolute, gemessene!
Naja, wenn alle Messungen perfekt sind dann kann es wohl nur noch ein Naturwunder sein. Was soll man da noch sagen.
- Timmopheus
- Illumina-Mitglied
- Beiträge: 919
- Registriert: Donnerstag 24. Juli 2008, 17:13
-
CD-ROM-LAUFWERK
- Illumina-Mitglied
- Beiträge: 581
- Registriert: Sonntag 5. Januar 2014, 23:05
Ich bin dann doch eher auf der Suche nach bodenständigeren ErklärungenNaja, wenn alle Messungen perfekt sind dann kann es wohl nur noch ein Naturwunder sein. Was soll man da noch sagen.
Etwa das mit der Kondensationshemmung, von der ich bislang noch nicht mal etwas gehört hatte.
Ja, es gibt viele Programme, mit denen man eine Funktion fitten lassen kann und dann gucken kann, ob es was taugt usw. usf.kann man jede erdenkliche Funktion selbst definieren und fitten lassen.
Ist der zugrundeliegende Verlauf (also etwa die Theorie dahinter) unklar, dann nützt das praktisch nichts. Etwa wenn ich den Wärmestrom real mit einem theoretischen Modell fitten will und dabei die Wärmestrahlung nicht einbeziehe, weil ich/man von ihr (angenommen) noch nichts weiß. Oder der Reaktionsmechanismus einer Reaktion ist unbekannt oder wenn doch, dann viel zu kompliziert und muss empirisch (vereinfacht) modelliert werden, damit man nicht 30 Reaktionsgeschwindigkeitskonstanten hat, von denen 20 nur sehr sehr schwer zu bestimmen wären.
Tablecurve 2D fittet (in wenigen Sekunden) mehrere tausend gängige Gleichungen. Man kann diese dann sortieren und direkt die Qualität (als Zahl und grafisch) beurteilen. Das ist so unglaublich viel effizienter als mit Excel oder sonstiges "einzeln-fitten", das konnte ich mir vorher nicht vorstellen. Dabei ist das Programm ursprünglich von 1989 - tortzdem habe ich keine Alternative gefunden. Dank der 30 Tage Testversionen konnte ich viele Programme ausprobieren bzw. habe gecrackte Versionen getestet oder auch (ein)mal selbst gecrackt. Eigene Funktionen kann man dort selbstverständlich ebenfalls einpflegen. Wenn das hier gewünscht ist, würde ich sogar mal ein Tutorial o.ä. dazu erstellen und hochladen. Vermutlich mangelt es dafür jedoch an breiterem Interesse und es bleibt eher Thema für 2-3 Personen beim Usertreffen... oder jetzt neu im Discord?
Größer 0m. Aber ja, das ist so, ich wollte das in dem Zusammenhang nur erwähnt haben. Ich bin mal in diese "Falle" getappt, als ich die Daten einer "Wetterseite" genutzt hatte. Jedenfalls war der Luftdruck in dem Zeitraum (und an dem Ort) tatsächlich so hoch.Bei höhne < 0m (was in DE überwiegend der Fall ist) ergibt sich dabei ein rechnerisch höherer Luftdruck als der absolute, gemessene!
-
Glaskocher
- Illumina-Mitglied
- Beiträge: 2544
- Registriert: Dienstag 27. Oktober 2015, 22:17
- Wohnort: Leverkusen
Bevor wir uns noch über den Einfluss der Mondphasen auf die Siedeeigenschaften unterhalten wiederhole ich nochmal meine Frage vom 02 Jan 2017 21:13. Über die Reinheit der eingesetzten Stoffe und das Protokoll vom Destillationsverlauf (Kopftemperatur in Abhängigkeit von Zeit oder besser Destillatmenge) haben wir bisher noch nicht nachgedacht.Ich bin dann doch eher auf der Suche nach bodenständigeren Erklärungen
- mgritsch
- Illumina-Admin
- Beiträge: 4385
- Registriert: Montag 8. Mai 2017, 10:26
- Wohnort: in den Misanthropen
sorry, da war ich gerade am Sprung und habe Kauderwelsch geschrieben, incl. Typos.CD-ROM-LAUFWERK hat geschrieben:Größer 0m. Aber ja, das ist so, ich wollte das in dem Zusammenhang nur erwähnt haben. Ich bin mal in diese "Falle" getappt, als ich die Daten einer "Wetterseite" genutzt hatte. Jedenfalls war der Luftdruck in dem Zeitraum (und an dem Ort) tatsächlich so hoch.Bei höhne < 0m (was in DE überwiegend der Fall ist) ergibt sich dabei ein rechnerisch höherer Luftdruck als der absolute, gemessene!
Natürlich ist klar dass man in DE meist auf einer Höhe >0m ist (es sei denn man nähert sich zu sehr den Niederlanden oder besucht im Ruhrpott einen tiefen Kohleschacht...) und jedenfalls kann der tatsächliche, physische Luftdruck gegenüber dem rechnerisch korrigierten nur niedriger liegen (so von wegen mir erschienen deine 1031 mbar etwas hoch... )
Ad Kondensationshemmung: die bekannteste praktische Anwendung ist die Nebelkammer...
Muss aber gar nicht bis ganz zum unterkühlten Dampf gehen - sollte sich rund um das Thermometer Aerosol zeigen dann ist bereits eine Kondensation im Gange weil es dort wohl irgendwo eine "Kältebrücke" gibt und die Temperatur kann etwas niedriger liegen als theoretisch erwartet. Das wäre soweit meine einzige Theorie - falls wir davon ausgehen dass deine Messgeräte perfekt sind und das Naturwunder ausgeschlossen ist. Ich sehe (abgesehen von der von Glaskocher erwähnten Verunreinigung der Stoffe) keine andere Variable mehr im System außer "Ungleichgewicht". Unter "Verunreinigung" könnte dabei auch ein höherer Wassergehalt als dem Azeotrop entsprechend fallen.
-
CD-ROM-LAUFWERK
- Illumina-Mitglied
- Beiträge: 581
- Registriert: Sonntag 5. Januar 2014, 23:05
Okay, aber da gibt es keine Oberfläche sondern nur die Gasphase, die in sich sicherlich deutlich gehindert ist.Ad Kondensationshemmung: die bekannteste praktische Anwendung ist die Nebelkammer...
Tröpfchen o.ä. waren nicht zu beobachten.
Über die Reinheit kann ich keine definitiven Aussagen machen. Aber da werden keine Verunreinigungen mit einem etwas unter EtOH liegenden Siedepunkt drin sein. Siehe auch die andere Destillation von reinem Wasser.
Zum Destillationsverlauf: man sieht deutlich, wenn ich mal etwas am Rücklauf spiele. Anfangs ging es mir zu langsam, daher der erste Temperatursprung (13min) von ~77,4°C auf ~78,2°C. Dann noch mal ein Sprung (37min) auf ~78,4°C. Dann später habe ich den Rücklauf immer mal wieder erhöht, damit weniger Wasser über geht. Daher geht auch die Geschwindigkeit runter (rot flacht ab).
Ich würde das Ganze auch wiederholen, dann gerne auch nur mit "reinem" Ethanol. Aber das Ergebnis wird identisch sein, wie schon bei der Destillation von Wasser. Da passt der Druck auch nicht zur gemessenen Temperatur:


- mgritsch
- Illumina-Admin
- Beiträge: 4385
- Registriert: Montag 8. Mai 2017, 10:26
- Wohnort: in den Misanthropen
eine NebelKAMMER hat wohl schon Oberfläche (auch wenn sie gerne zwecks Beobachtung transparent ausgeführt ist), sonst würde sich der Nebel recht schnell verziehen...CD-ROM-LAUFWERK hat geschrieben:Okay, aber da gibt es keine Oberfläche sondern nur die Gasphase, die in sich sicherlich deutlich gehindert ist.
Nota bene: "Eine Nebelkammer ist meist mit einem übersättigten Luft-Alkohol-Gemisch (Ethanol oder Isopropanol) gefüllt." (https://de.wikipedia.org/wiki/Nebelkammer) --> Hinweis auf eine speziell erhöhte Neigung zur Unterkühlung bei Alkohol?
Sonst: Wenn die Richtigkeit der Messung schon nicht so leicht zu beurteilen ist - wie sieht es mit der Reproduzierbarkeit aus? Wenn du an verschiedenen Tagen mit jeweils frisch angesetztem Mix EtOH-Wasser und leicht anderen Druck-Bedingungen das Experiment wiederholst - bekommst du dann ein einigermaßen konstantes "Offset" zum errechneten Wert? Oder schwankt das dann auch schon unvorhersehbar?
wenn du von den verschiedenen Seiten kommst und einmal mit abs. einem Mix über und einmal unter azeotroper Mischung startest, ändert das etwas am Ergebnis (abolut oder relativ)?
wenn du ein anderes System betrachtest wo ein Maximum-Azeotrop vorliegt (zB Chloroform/Methanol), ändert das etwas am Ergebnis (abolut oder relativ)?
Verunreiningungen: benutzen noch andere Leute diese Kolonne und hinterlassen darin evtl etwas, und sei es nur Reinigungsmittel?
Apparatur: kannst du die Temperatur an verschiedenen Stellen messen (fühler mal ein paar cm runter oder rauf...) - was ändert sich dann?
Darf ich mal am Rande ganz ketzerisch fragen welche Relevanz eine Temperaturabweichung von der ideal-Erwartung um ein paar 10tel ° hat?
Rein akademisches Interesse an der Nachvollziehbarkeit oder leitet sich daraus irgend etwas ab?
-
CD-ROM-LAUFWERK
- Illumina-Mitglied
- Beiträge: 581
- Registriert: Sonntag 5. Januar 2014, 23:05
Weitere Tests muss ich dann halt mal machen, wenn Zeit ist.
Die Temperaturdifferenz beträgt immerhin 1,25°C.
Es handelt sich um rein akademisches Interesse, diese Beobachtungen zu erklären. Ob sich daraus relevante Informationen für die Zukunft ableiten lassen? Wird sich erst hinterher zeigen...
Die Temperaturdifferenz beträgt immerhin 1,25°C.
Ja, selbstverständlich. Aber es gibt so gut wie keine Strömungen sondern ruhige Gasschichten. Durch Wärmeleitung (keine Konvektion) kann dann etwas unterkühlen.hat wohl schon Oberfläche
Es ist eine normale Füllkörperkolonne. Ich könnte höchstens noch irgendwie unten im Kolben messen. Irgendwie, da ich keinen 4 Liter 2-Hals Kolben habe.Apparatur: kannst du die Temperatur an verschiedenen Stellen messen (fühler mal ein paar cm runter oder rauf...) - was ändert sich dann?
Es handelt sich um rein akademisches Interesse, diese Beobachtungen zu erklären. Ob sich daraus relevante Informationen für die Zukunft ableiten lassen? Wird sich erst hinterher zeigen...